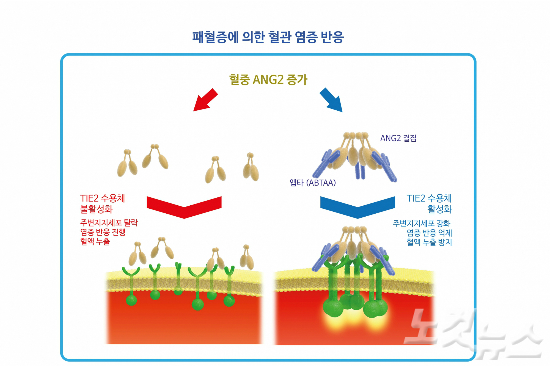
 패혈증에 의한 혈관 염증 반응시 앱타의 작용 모식도. (사진=IBS 제공)
패혈증에 의한 혈관 염증 반응시 앱타의 작용 모식도. (사진=IBS 제공)
기초과학연구원(IBS) 혈관연구단(단장 고규영 KAIST 의과학대학원 특훈교수)은 패혈증의 진행과 치료의 새로운 혈관표적(TIE2)을 발견하고, 이를 활성화하면 패혈증 악화에 강력한 억제효과를 얻을 수 있다는 연구결과를 21일 발표했다.
패혈증은 치사율이 높은 질병 가운데 하나이지만, 강력한 표적치료제가 없어 치료에 어려움을 겪어 왔다. 기존 연구에서는 모세혈관 파괴로 인한 주요 장기 기능 저하를 주요 사망 원인인 것으로 추정해 왔으나, 그 진행과정을 명확히 규명하지 못해 표적치료제 개발에도 난항을 겪었다.
연구진은 패혈증의 진행과정에서 혈관 손상과 혈액 누출을 억제해야 한다는 사실에 주목해 혈관내피세포의 TIE2 수용체와 관련 단백질(ANG2)의 역할을 집중적으로 살펴봤다.
TIE2 수용체는 미세혈관을 안정화시키고 보호하는 반면, 혈액 내 ANG2 단백질은 TIE2 수용체에 특이하게 결합해 혈관을 불안정하게 만들고 누출을 유발하기 때문.
혈관내피세포의 항상성을 연구한 결과, ANG2 단백질의 작용을 억제하면서 TIE2 수용체를 활성화하면 혈관 강화 과정을 통해 혈액 누출을 막을 수 있을 것이라고 내다봤다.
즉, 패혈증 초기 진행과정에서 일어나는 혈관내피세포의 TIE2 수용체 단백질 감소와 기능 저하가 주요장기 미세혈관 손상, 혈액 누출, 혈관 염증의 주요 원인이며, 이 과정에서 TIE2 수용체의 활성을 강화한다면 혈관내피세포의 파괴 현상을 막아 패혈증의 치명적 결과를 막을 수 있다는 가설을 세우고 이를 검증한 것이다.
연구진은 이를 위해 혈관 손상을 예방하면서 동시에 혈관을 강화하는 새로운 개념의 이중 작용 실험적 항체인 '앱타'(ABTAA, ANG2-Binding and TIE2-Activating Antibody)를 개발했다.
앱타는 표적 물질인 ANG2 단백질에 결합해 ANG2 단백질에 의한 혈관 손상을 예방할 뿐만 아니라, ANG2 단백질을 결집시켜 TIE2 수용체를 활성화 시키는 독특한 이중 기능을 지녔다. 마치 적을 친구로 만드는 것처럼 ANG2 단백질의 역기능을 순기능으로 바꾸는 셈이다.
연구진이 패혈증에 걸린 실험동물에 앱타를 적용한 결과, 폐와 신장에서 일어나는 혈액 누출과 혈관 손상, 염증 반응, 부종 등이 감소하면서 생존율이 현저히 향상되는 것으로 확인됐다.
패혈증에 걸린 실험동물은 조치를 취하지 않은 경우 80시간 이내에 모두 폐사했으나, 앱타를 투여한 경우에는 30% 이상의 생존율을 보였다. 특히 앱타를 항생제와 함께 투여한 실험동물은 70% 정도까지 생존율이 높아진 것으로 나타났다.
물론, 앱타는 아직 실험적인 항체이기 때문에 임상적용을 위해서는 보다 많은 개발이 필요하다는 게 연구진의 설명.
고규영 단장은 "이번 연구는 탄탄한 기초연구가 난제의 패혈증 연구와 치료 방향에 도움을 줄 수 있다는 것을 보여준 사례"라며 "메르스, 에볼라 등 신종 바이러스 감염과 각종 박테리아 감염 등으로 인해 필연적으로 발생하는 패혈증 치료에 혈관 TIE2 활성제가 추가 선택치료 약물로 사용되기를 희망한다"고 말했다.
이번 연구결과는 '사이언스 중개 의학'(Science Translational Medicine, IF=15.8) 온라인에 실리면서 표지를 장식했다.