 모더나 백신. 연합뉴스
모더나 백신. 연합뉴스미국 식품의약국(FDA)이 자국 모더나 사(社)가 제조한 코로나19 백신이 '부스터샷'(효과 보강을 위한 추가접종)에 다소 적합하지 않다는 판정을 내린 가운데 정부가 향후 미국 당국이 접종기준을 변경할 경우 충분히 관련내용을 검토하겠다고 밝혔다.
북유럽 국가들에 이어 인접한 일본도 젊은층 남성들에게 심근염·심낭염 등의 부작용을 이유로 모더나 접종을 권고하지 않기로 한 데 대해서도 사례들을 좀 더 수집해 전문가 심의를 거치겠다는 입장이다.
코로나19 예방접종대응추진단(추진단) 홍정익 예방접종관리팀장은 14일 브리핑에서 모더나 부스터샷에 부정적인 입장을 나타낸 미국 보건당국을 두고 "미국 FDA와 질병통제예방센터(CDC)에서 모더나와 얀센 백신 추가접종에 대한 접종 대상자, 접종용량 등 접종기준에 대한 공식적인 정책이 발표되면 그 부분에 대해 충분히 검토할 예정"이라고 말했다.
그러면서 "그간 모더나와 얀센 백신 추가접종에 대한 축적된 연구결과를 바탕으로 전문가 자문 및 예방접종자문위원회의 심의를 통해 충분히 고려해 결정하겠다"고 부연했다.
로이터통신 등 외신에 따르면, FDA는 지난 12일(현지시각) 공개한 문건을 통해 모더나 백신을 2차례 맞는 기본접종만으로도 코로나 예방효과가 강하게 지속된다고 밝혔다.
또 부스터샷을 맞으면 항체가 더 늘어날 수는 있지만, 추가접종 전후의 항체 수준에 유의미한 차이가 없다며 특히 많은 항체를 보유한 접종자들의 경우 이러한 현상이 나타난다고 지적했다.
이같은 내용은 FDA의 외부 자문기구인 백신·생물의약품자문위원회(VRBPAC)가 14~15일 모더나, 존슨앤드존슨 사의 얀센 백신에 대해 부스터샷 필요 여부를 논의하기로 한 가운데 공개됐다. 미국 CDC는 FDA가 모더나의 부스터샷을 승인할 경우 접종 권고대상과 관련해 다음 주 회의를 열기로 한 상황이다.
 지난 6월 충북 청주시의 GC녹십자 오창공장에 입고된 모더나 백신. 사진공동취재단
지난 6월 충북 청주시의 GC녹십자 오창공장에 입고된 모더나 백신. 사진공동취재단앞서 모더나 측은 4주 정도의 간격을 두고 2회 접종되는 자사 백신의 투여량을 절반으로 줄여 65세 이상 고령층과 고위험군에 1차례 더 접종하는 부스터샷을 시행하겠다며 승인을 요청했다.
하지만 FDA 내부에서는 부스터샷의 필요성을 뒷받침하는 근거가 화이자 백신으로 추가접종을 실시한 이스라엘에서 나왔다는 점, 모더나와 얀센 측이 충분한 근거자료를 제공하지 않았다는 점도 문제삼고 있는 것으로 알려졌다.
현재 모더나는 면역저하자, 60세 이상 고령층 등을 대상으로 하는 국내 4분기 부스터샷에 쓰이는 백신이기도 하다. 정부는 항체 형성에 어려움을 겪는 면역저하자 등만을 제외하고는 화이자나 모더나 등 mRNA(메신저 리보핵산) 백신을 접종완료한 지 6개월이 지난 시점에 mRNA 백신을 추가접종하는 방안을 진행 중이다.
1회 접종으로 접종이 완료되는 얀센 접종자들도 예방접종 후 6개월이 되는 12월부터 mRNA 백신에 의한 부스터샷이 유력한 상태다.
이와 별개로 스웨덴 등 일부 북유럽 국가에 이어 일본이 당분간 10~20대 남성에 대해 모더나가 아닌 화이자 접종을 권고하기로 한 결정도 논란이 되고 있다. 심근염·심낭염 발생률이 상대적으로 더 높다는 우려에서다.
일본에서는 모더나 백신 접종 후 심근염 의심증상이 나타난 10대 남성이 14.49건, 20대 남성이 100만 회당 10.4건 꼴로 보고된 것으로 파악됐다. 반면 화이자 백신은 10대 남성이 100만 회당 1.3건, 20대는 100만 회당 8.15건 정도로 나타났다.
이에 대해 홍 팀장은 "관련해서 자료를 수집 중에 있다. 국가 정책동향도 관찰하고 있다"며 "아직 정해진 바는 없지만 국내·외 심근염·심낭염 신고와 해외 부작용 현황, 국외 접종기준 변경 등 관련자료를 정리해 전문가 자문과 예방접종전문위의 심의를 통해 논의할 예정"이라고 말했다.
앞서 스웨덴은 지난 6일 30세 이하 연령층에 대한 모더나 접종을 일시 중단했고, 덴마크도 같은 날 12~17세의 접종 백신을 화이자로 제한하겠다고 발표했다. 핀란드 또한 예방적 차원에서 30세 이하 젊은층에게 화이자 백신만을 맞히겠다고 밝혔다.
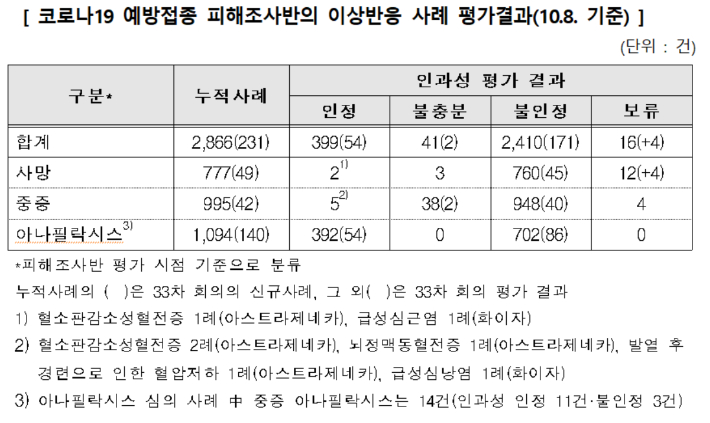 코로나19 예방접종대응추진단 제공
코로나19 예방접종대응추진단 제공 한편, 지난 8일 열린 예방접종피해조사반(반장 김중곤 교수)의 33차 회의에서는 '백신 이상반응' 231건에 대한 심의가 이뤄졌다. 각각 사망 49건, 중증 42건, 중증 전신 알레르기 반응인 '아나필락시스' 140건이 새롭게 접수됐고, 사망사례 2건도 재심 안건에 올랐다.
피해조사반은 이 중 아나필락시스 54건에 대해서만 백신 접종과 부작용 사이 인과성을 인정한 것으로 파악됐다. 급성심근염 등 중증 2건은 판단근거라 불충분한 사례로 평가됐다.
신규 사망신고(49건)의 평균 연령은 73.6세로 나타났다. 이 가운데 85.7%(42건)는 고혈압, 당뇨, 고지혈증 등의 기저질환이 있었던 것으로 조사됐다.
접종 백신은 아스트라제네카(AZ) 25건, 화이자 14건, 모더나 8건, 얀센과 교차접종이 각각 1건씩이다.
중증사례(42건)의 평균 연령은 68.9세(범위 17~99세)로 71.4%(30건)는 기저질환 보유자인 것으로 파악됐다. 백신을 맞고 증상이 나타나기까지 평균 10.6일이 소요됐다.
이들이 접종한 백신은 AZ 백신 19건, 화이자 13건, 모더나 8건, 교차접종 2건이었다.